மெண்டெலீவின் தனிம வரிசை அட்டவணை
1869 - ல் இரஷிய வேதியியலாளர் டிமிட்ரி மெண்டலீவ் தனிமங்களின் பண்புகள், அவை அணு நிறையின் அடிப்படையில் எடுக்கப்படும் போது ஒரு குறிப்பிட்ட இடைவெளிக்குப் பிறகு மறுபடியும் வருவதைக் கண்டறிந்தார். இதன் அடிப்படையில் இவர் தனிம ஆவர்த்தன விதியை உருவாக்கினார்.
மெண்டெலீவின் ஆவர்த்தன விதி :
" தனிமங்களின் இயற்பியல் மற்றும் வேதியியல் பண்புகள் அவற்றின் அணுநிறைகளை பொருத்து ஆவர்த்தன முறையில் மாற்றம் அடைகிறது. "
மெண்டலீவ் அந்த நேரத்தில் அறியப்பட்ட 56 தனிமங்களை இந்த விதியின் அடிப்படையில் அமைத்தார்.
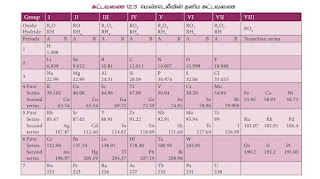
மெண்டெலீவ் தனிம வரிசை அட்டவணையின் சிறப்புகள்:
1. இதில் 8 நீண்ட செங்குத்து தொகுதிகளும் ஏழு கிடைமட்ட தொடர்களும் காணப்படுகின்றன.
2. தொடர்கள் ஒவ்வொரு தொகுதிக்கும் இரண்டு துணைத் தொகுதிகள் A மற்றும் B உள்ளது.
3. ஒரு தொகுதியில் காணப்படும் எல்லா தனிமங்களும் ஒத்த பண்பினைக பபெற்றிருக்கும்.
4. முதன் முறையாக தனிமங்கள் விரிவாக சரியான முறையில் வகைப்படுத்தப்பட்டன. இதனால் ஒத்த பண்புகளை உடைய தனிமங்கள் ஒரே தொகுதியில் வைக்கப்பட்டன.
5. ஒத்த பண்புகளை உடைய தனிமங்கள் ஒரே தொகுதியில் வைக்கப்பட்டு வகைப்படுத்தப்பட்ட போது சில தனிமங்கள் அவற்றிற்கான தொகுதியில் வைக்கப்பட முடியாமல் போனது கண்டறியப்பட்டது. ஏனெனில் அவற்றிற்கு தீர்மானிக்கப்பட்ட அணு நிறை தவறாகும். இது கண்டறியப்பட்டு பின்னர் இந்த தவறு சரிசெய்யப்பட்டது.
எ. கா : முதலில் பெரிலியத்தின் அணு நிறை 14 என அறியப்பட்டத. இதை மறுபடியும் ஆராய்ந்து அணு நிறை 9 எனக் கண்டறிந்து சரியான தொகுதியில் அதை வைத்தார்.
6. அந்த நேரத்தில் கண்டுபிடிக்கப்படாத தனிமங்களுக்கு என்று அட்டவணையின் பத்தியில் காலியிடம் விடப்பட்டது. அவற்றின் பண்புகள் கூட முன்னறியப்பட்டதாக அமைததது.
எ. கா: அலுமினியம் மற்றும் சிலிக்கானுக்குகக் கீழே வரக்கூடிய நிருபிக்க தனிமங்களுக்கு ஈ.கா அலுமினியம் மற்றும் ஈ.கா சிலிக்கான் எனப் பெயரிட்டார். மேலும் அவற்றின் பண்புகள் இவ்வாறுதான் இருக்கும் என முன்னறிவித்தார். அவரது காலத்தில் காலத்திலேயே பின்னர் கண்டுபிடிக்கப்பட்டது ஜெர்மானியம்அவரின் கூற்று சரி என நிரூபித்தது.
குறைகள் :
1. பண்புகளில் அதிக வேறுபாடுள்ள தனிமங்களும் ஒரே தொகுதியில் வைக்கப்பட்டன.
எ. கா : கடின உலோகங்களாகிய செம்பு மற்றும் வெள்ளி, மென் உலோகங்களாகிய சோடியம் மற்றும் பொட்டாசியத்தோடு ஒரே தொகுதியில் வைக்கப்பட்டன.
2. ஹைட்ரஜனுக்கு என்று ஒரு தனி இடம் கொடுக்கப்பட முடியவில்லை. அலோகமாகிய ஹைட்ரஜன், மென் உலோகங்களாகிய லித்தியம், சோடியம் மற்றும் பொட்டாசியம் போன்றவற்றுடன் ஒரே தொகுதியில் வைக்கப்பட்டன.
3. கூடிக்கொண்டே செல்லும் அணு நிறை எனும் விதியை சில வேளைகளில் கடைபிடிக்க முடியவில்லை. எ. கா : CO & Ni, Te & I.
4. ஐசோடோப்பு களுக்கு தனியாக இடம் ஒதுக்கப்படவில்லை.


கருத்துகள்
கருத்துரையிடுக